| chlorure de fer [23811] |
|
| Posté le : 30/09/2006, 11:46 (Lu 8783 fois) |
bonjour a tous!
j'ai un petit problème...
après réaction entre acide chlorhydrique et limaille de fer et filtrage, je sépare la solution en deux tubes à essais :
- dans le premier j'ajoute de la soude
- dans le second j'ajoute de l'ammoniac
tube 1 : obtention d'un précipité blanc
tube 2 : obtention d'un précipité rouille puis vert foncé après ajout d'eau distillée
je voudrais savoir pourquoi j'obtiens ça et pas un précipité vert avec la soude ( Fe(OH)2 ) et des vapeurs blanches avec l'ammoniac ( NH4Cl ) ?
merci d'avance pour votre réponse 
| |
|
|
| Re: chlorure de fer [23812] |
|
| Posté le : 30/09/2006, 12:20 (Lu 8779 fois) |
PS : je dois normalement obtenir du chlorure de fer II 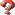
| |
|
|
| Re: chlorure de fer [23913] |
|
| Posté le : 01/10/2006, 17:27 (Lu 8737 fois) |
Quand on attaque le fer par HCl, on obtient une solution de chlorure de fer(II) FeCl2.
Fe + 2 HCl ---> H2 + FeCl2
Mais cette solution s'oxyde peu à peu à l'air, selon :
4 Fe + 4 H+ + O2 --> 4 Fe3+ + 2 H2O.
Donc ta solution contient simultanément Fe2+ et Fe3+, en quantités très variables.
Quand tu ajoutes une solution de NaOH ou de l'ammoniaque (c'est égal - voir plus bas), les deux ions de fer vont réagir. Mais le fer(III) réagit avec le fer(II). Tu provoques d'abord la formation d'un précipité rouille d'hydroxyde de fer(III) Fe(OH)3, puis un précipité vert d'hydroxyde de fer(II) Fe(OH)2.
Fe3+ + 3 OH- --> Fe(OH)3
Fe2+ + 2 OH- --> Fe(OH)2
NaOH forme des ions OH-. L'ammoniaque NH3 forme aussi des ions OH-, par réaction avec l'eau, selon :
NH3 + H2O --> NH4+ + OH--
Selon la proportion du fer(II) qui s'est oxydée, tu verras mieux la formation de l'un que l'autre de ces deux hydroxydes.
----------
Edité le 01/10/2006 à 21:08 par Unkky
|
Professeur de chimie de niveau préuniversitaire
|
|
|
| Re: chlorure de fer |
|
| Posté le : 03/10/2006, 19:04 (Lu 8680 fois) |
si la solution s'oxyde à l'air .... on peu s'arranger pour na pas voir d'air (mettre un anti-retour à la sortie d'un ballon juste avant la réaction) il ne reste donc que la solution de chlorure de fer et comme gaz de l'hydrogéne ....
Ensuite, on fait chauffer pour faire évaporer l'eau (ce qui, je pense n'est pas dangereux de chanffer H2 car il n'y a pas d'O2) et on pourrai ainsi récupérer les chlorures de fer sous forme de cristaux ?
Je pense bien sur que j'ai faux, ce serait trop facile ...
Mais svp dites moi où j'ai faux ? 
| |
|
|
| Re: chlorure de fer [24046] |
|
| Posté le : 03/10/2006, 18:09 (Lu 8690 fois) |
merci !  
| |
|
|
| Re: chlorure de fer [50138] |
|
| Posté le : 12/10/2007, 14:19 (Lu 7583 fois) |
Citation
on peu s'arranger pour na pas voir d'air |
|
Tout le monde a compris mais c'est quand même un joli pléonasme que de s'assurer de ne pas voir de l'air ( l'air ne se voit pas    ) )
| |
|
|
Aztek Forum V4.00 Copyright (C) 2003 |